2023年2月10号,华夏源(上海)生物科技有限公司自主研发的I类生物制品,“ELPIS人脐带间充质干细胞注射液”(受理号:CXSL2200581),正式获得国家药监局药品审评中心(CDE)的药物临床试验批准通知(通知书编号:2023LP00238),予以准许开展Ib期临床试验。
新适应症主要用于慢加急性(亚急性)肝衰竭的治疗,这是继华夏源“ELPIS人脐带间充质干细胞注射液”中、重度斑块型银屑病和重度狼疮性肾炎适应症获批后斩获的又一新适应症,这是华夏源干细胞新药产品的第三个应用方向,也将为慢加急性(亚急性)肝衰竭带来新的治疗选择。
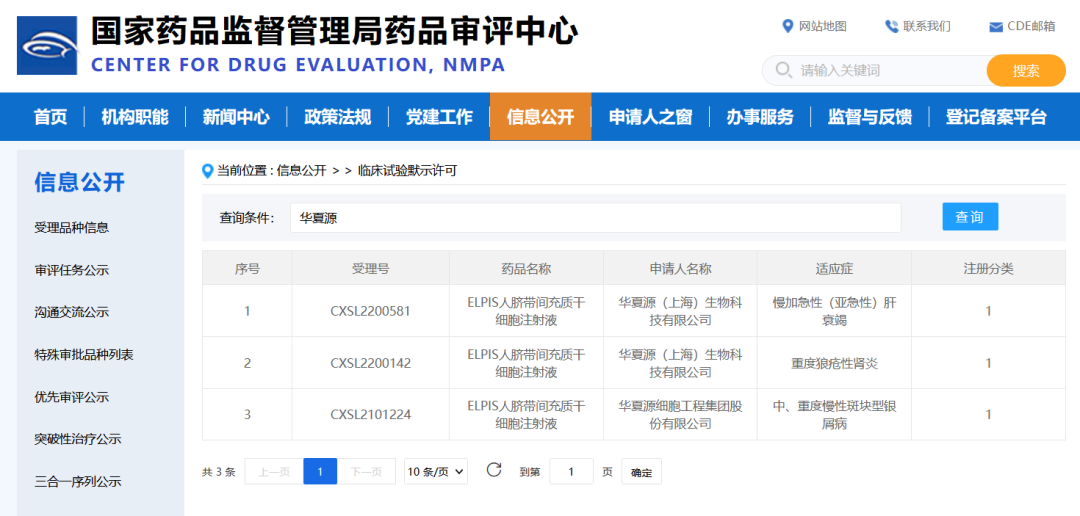
△ 国家药监局官网:华夏源“ELPIS人脐带间充质干细胞注射”获临床试验默示许可

△ 国家药品监督管理局药物临床试验批准通知
CDE,即国家药品监督管理局药品审评中心,是国家食品药品监督管理局药品注册技术审评机构,按照国家食品药品监督管理局颁布的药品注册管理有关规章,负责组织对药品注册申请进行技术审评,组织开展相关的综合评审工作。
IND,即新药临床试验,是药物研发企业以注册目的,在药品正式上市前,向CDE提供足够信息来证明药品在人体进行试验是安全的,以及证明针对研究目的的临床方案设计是合理的而开展的人体临床试验。
我国是肝病大国,每年早、中期肝衰竭病人超百万,晚期病人约45万,其中慢加急性(亚急性)肝衰竭(ACLF)占肝衰竭的70%-80%,发病呈逐年上升趋势,ACLF患者体内产生的大量促炎因子,将导致机体出现系统性炎症反应综合征(SIRS),SIRS是ACLF高死亡率的重要原因,减少促炎因子和坏死的肝细胞是治疗ACLF的关键。
目前,ACLF的内科治疗尚缺乏特效药物和手段,原则上强调早期诊断、早期治疗,采取相应的病因治疗和内科综合治疗措施,并积极治疗并发症。人工肝治疗可为肝细胞再生及肝功能恢复创造条件,是目前治疗ACLF的有效方法之一,但却不能逆转肝细胞数量日益减少所导致的肝功能减退;肝移植作为目前救治肝衰竭成功率最高的治疗措施,由于肝源不足、费用高昂、需要长期抗排异治疗等原因也存在一定的局限性。
干细胞治疗是通过移植来替换、修复患者损伤的细胞,或发挥免疫调节、组织修复等功能,以到达治疗疾病的目的。
ELPIS人脐带间充质干细胞基于其免疫调节功能,可抑制多种过度激活的免疫细胞,保持免疫平衡,改善免疫细胞过度活化导致炎症因子大量释放;其次ELPIS可以通过旁分泌、免疫调节作用减轻肝脏炎症反应并调节肝星状细胞的增殖和凋亡,减少胶原的沉积从而减轻肝脏纤维化改善肝脏的微环境;并通过HGF、VEGF等因子的分泌抑制肝细胞凋亡以促进肝再生,从而发挥一个“组织修复的作用”。
因此,ELPIS人脐带间充质干细胞可以在肝脏坏死的“急性治疗”期作为桥接手段发挥免疫调节及促进肝脏再生的“过渡”作用,也可在恢复期辅助其他治疗,减少肝纤维化、肝硬化的发生。ELPIS人脐带间充质干细胞的这些作用特点决定了其治疗ACLF的优势。
